Лед вода это система гомогенная
19.1. Фазы
При описании многих физических и химических систем используется понятие фаза.
Фаза – часть системы, однородная по составу и строению и отделенная от других частей системы (других фаз) границей раздела (межфазной границей).
Фазой системы может быть газ или смесь газов, жидкость (или жидкий раствор), твердое вещество (или твердый раствор). В любом случае, чтобы представлять собой отдельную фазу, такая составная часть системы должна быть однородной. Каждое из твердых веществ и каждая из несмешивающихся жидкостей представляют собой отдельную фазу.
Система, образованная водой и таящим льдом, состоит из двух фаз, так как, хоть по составу вода и лед одинаковы, у них разное строение, кроме того, между ними есть граница раздела. Воздух, соляная кислота, подкисленный серной кислотой водный раствор перманганата калия – системы, состоящие из одной фазы; здесь нет границ раздела, и в любой части такой системы состав и строение одинаковы.
В приведенном определении понятия » фаза» есть некоторые особенности, не дающие считать это определение исчерпывающим. Это, прежде всего, требование одинаковости состава и строения фазы. Оно относится только к фазам равновесных систем. Если в системе происходит химическая реакция, или просто растворение твердого вещества в жидкости, то фаза может быть и не однородна. Кроме того, сравниваемые объемы однородной фазы не должны быть соизмеримы с размером частиц (молекул, ионов), из которых состоит данная фаза – в противном случае, любая фаза окажется неоднородной. Другие проблемы, связанные с понятием » фаза» , рассматриваются в ВУЗах при изучении курса физико-химического анализа.
По числу фаз системы делят на гомогенные и гетерогенные.
| Гомогенная система – система, состоящая из одной фазы. Гетерогенная система – система, состоящая из двух или большего числа фаз. |
Фаза может быть сплошной или дисперсной (раздробленной на множество отдельных частиц). Сплошной фазой принято считать фазу, из любой точки которой можно попасть в любую другую точку, не пересекая межфазную границу.
Гомогенная система может быть образована лишь сплошной фазой.
Гетерогенная система может быть образована, как сплошными, так и дисперсными фазами.
Вода с помещенной в нее цинковой пластиной представляет собой гетерогенную систему, состоящую из двух сплошных фаз; если же в ту же воду насыпать цинковую пыль, или просто поместить отдельные гранулы цинка, то в такой системе одна из фаз будет дисперсной.
Сплошные фазы гетерогенных систем (а иногда и гомогенных) часто называют срe дами, например: » жидкая среда» , » твердая среда» , » водная среда» и т. п.
19.2. Дисперсные системы
Гетерогенные системы, содержащие дисперсные фазы называют дисперсными системами. При этом сплошная фаза дисперсной системы называется дисперсионной средой.
Названия некоторых дисперсные систем с различными агрегатными состояниями дисперсионной среды и дисперсной фазы приведены в таблице 2.
Агрегатное состояние
Агрегатное состояние дисперсной фазы
дисперсионной среды
Жидкость
Дымы, пыли, порошки
Жидкость
Эмульсии
Суспензии, пасты
Твердые пены
Туманы и дымы носят общее название – аэрозоли. Именно они (в данном случае туманы) образуются при выпускании в воздух содержимого аэрозольных баллончиков. Дымы образуются не только при горении топлива, но и в результате многих других химических реакций, например, при взаимодействии хлороводорода с аммиаком.
К эмульсиям относится обычное молоко и множество технических эмульсий, например, применяемых для смазки и охлаждения режущего инструмента (эмульсии машинного масла в воде).
Примером грубодисперсной суспензии служит строительный » раствор» (суспензия песка и цемента в воде), а мелкодисперсной – масляная краска (суспензия пигмента в олифе). При затвердевании строительного раствора и » высыхании» масляной краски они превращаются в дисперсные системы с твердой дисперсионной средой. К этой же группе дисперсных систем относятся некоторые сплавы и многие горные породы.
Примеры жидких пен – мыльная, пивная, квасная и другие пены. Твердыми пенами являются пенопласт, пенополиэтилен, пенополиуретан, некоторые строительные материалы-утеплители. В отличие от них, обычная банная губка является дисперсной системой с двумя взаимопроникающими дисперсионными средами. В виде дисперсных систем с жидкой дисперсной фазой и твердой дисперсионной средой выпускаются некоторые лекарственные средства.
Пользуясь терминологией, приведенной в этом параграфе, следует помнить о том, что она не всегда правильно используется, особенно в технике. Так строительный » раствор» – отнюдь не раствор, а грубодисперсная суспензия. Фотографическая » эмульсия» – отнюдь не эмульсия, а дисперсная система с твердой дисперсной фазой (в черно-белой фотографии – бромидом серебра) и твердой дисперсионной средой, основным компонентом которой является животный белок коллаген. Водоэмульсионная краска (правильное название – водно-дисперсионная) не является эмульсией, а представляет собой дисперсию в воде твердых частичек пигмента и связующего.
19.3. Коллоидные растворы
Истинные растворы – гомогенные системы. Частицы, из которых они состоят, перемешаны на атомно-молекулярном уровне. Кроме таких растворов существуют внешне однородные системы, содержащие очень мелкие частицы другой фазы, тем не менее не являющиеся отдельными молекулами или ионами. Такие гетерогенные системы носят название коллоидных растворов (более новое название – лиозоли).
Частицы в коллоидных растворах невозможно отделить фильтрованием. Если они и отстаиваются, то очень медленно (иногда для этого требуется несколько лет). Обычные центрифуги также, как правило, не позволяют разделить коллоидный раствор. Иногда это удается с использованием так называемых » ультрацентрифуг» – центрифуг с очень большой скоростью вращения. Такая устойчивость коллоидных растворов связана не только с незначительными размерами твердых частиц (примерно от 10 до 1000 Е), но и с довольно сложными электрофизическими явлениями на их поверхности, приводящими к взаимному отталкиванию коллоидных частиц.
 | Фаза, гомогенная система, гетерогенная система, сплошная фаза, дисперсная фаза, дисперсная система, дисперсионная среда, аэрозоль, эмульсия, суспензия, жидкая пена, твердая пена, коллоидный раствор (лиозоль). |


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Источник
Такая разная вода: два жидких агрегатных состояния H2O
Как нам всем известно в природе существует четыре основных агрегатных состояния вещества: твердое, жидкое, газообразное и плазма. Вода, будучи неотъемлемой составляющей и движущей силой жизни на планете, может при разных условиях пребывать в трех состояниях: в жидком, твердом (лед) и газообразном (пар). Однако ученые из Стокгольмского университета (Швеция) выяснили, что у воды имеется два разных жидких состояния. Первое мы наблюдаем на постоянной основе, а вот второе проявляется при температуре -63 °C. Как ученым удалось сделать это открытие, какими свойствами обладает вода во втором жидком состоянии, и какова его роль? Ответы на эти вопросы мы найдем в докладе ученых. Поехали.
Основа исследования
Фундаментом для подобного рода исследований стало обнаружение расхождения изотермической сжимаемости и теплоемкости (CP) при переохлаждении воды. Ученые начали поиски объяснений этих странных процессов.
Одна из самых распространенных теорий утверждает, что существует переход жидкость-жидкость (LLT от liquid-liquid transition) в переохлажденной воде между жидкостью высокой плотности (HDL от high-density liquid) и жидкостью низкой плотности (LDL от low-density liquid), который заканчивается в критической точке жидкость-жидкость (LLCP от liquid-liquid critical point) при положительном давлении. Аномальное поведение воды в соответствии с этой теорией объясняется колебаниями, исходящими от LLCP.
Относительно недавно были проведены дополнительные опыты, в ходе которых было обнаружено, что структура переохлажденной воды непрерывно изменяется при охлаждении до 227 К под давлением 1 бар. Это указывает на однофазное поведение без LLT при атмосферном давлении. Следовательно, это подразумевает, что если LLT действительно существует, то LLCP должен находиться при давлении (P) > 1 бар.
Эксперименты по рассеянию нейтронов в воде позволили предположить, что различные фазы HDL и LDL могут быть идентифицированы по их четко определенным положениям пиков в структурном факторе (математическое описание того, как материал рассеивает падающее излучение).
В частности, положение первого пика в О–О рассеянии сильно чувствительно к существованию тетраэдрических структур (LDL) или межузельных молекул между первой и второй оболочками (HDL). Следовательно, наиболее подходящим способом обнаружения LLT в переохлажденной воде может быть отслеживание структуры жидкости с помощью рассеяния рентгеновских лучей или нейтронов. Основная сложность таких опытов заключается в том, что их нужно проводить при разном давлении и очень быстро, пока не произошла кристаллизация.
В данном труде был использован метод компрессии-декомпрессии, когда начальное повышение давления было вызвано нагревом, индуцированным лазерным импульсом. Когда временной масштаб индуцированного лазером высвобождения энергии намного короче, чем время прохождения звука через образец, нагрев является изохорным*, а давление внутри образца значительно возрастает.
Изопроцесс* — термодинамический процесс, когда количество вещества и какой-то параметр его состояния (давление, объем, температура или энтропия) остаются неизменными.
После окончания сверхбыстрого лазерного импульса образец быстро расширяется по мере того, как внутреннее давление уменьшается, приближаясь к значениям давления окружающей среды. Однако, если динамика жидкости достаточно быстрая, чтобы расслабить образец до наступления расширения, квазиравновесное поведение будет наблюдаться во время процесса декомпрессии.
Образцы изучались с помощью рассеяния рентгеновских лучей с разными временными задержками во время декомпрессии. В ходе наблюдений было выявлено резкое изменение структурного фактора, которое указывает на прерывистый LLT. Кроме того была обнаружена кристаллизация льда, происходящая значительно позднее. Это подтверждает, что LLT является метастабильным состоянием и отличается от перехода жидкость-лед.
Результаты исследования
Аморфный лед* получают посредством быстрого охлаждения воды, так что ее молекулы не успевают сформировать кристаллическую решетку (т.е. молекулы расположены случайным образом).

Изображение №1
Толщина выбранных для наблюдения образцов варьировалась либо от 35 до 55 мм, либо от 15 до 25 мм. На образец воздействовал инфракрасный импульс с длиной волны 2 мм в течение 100 фс. Импульс увеличивал температуру и возбуждал комбинацию O–H и H–O–H.
ИК импульс с длиной волны 2 мм может перегреть и частично растопить лед за 10 нс. Такое частичное плавление наблюдалось для гексагонального образца льда (Ih) толщиной 100 мм (1B). Когда эквивалентный нагрев был применен к образцам HDA (толщиной 3 , а изохорный нагрев поддерживал плотность сразу после ИК-накачки. Измерение плотности и температуры переохлажденной воды в зависимости от давления после воздействия ИК импульса показало, что значения давления составляли от 2.5 до 3.5 кбар.
После активации ИК импульса началась самопроизвольная декомпрессия, во время которой температура оставалась примерно постоянной, пока через
100 мс охлаждение за счет теплопроводности не стало существенным.
Данная изотермическая декомпрессия снижала давление в образце. В этот момент проводили измерения с помощью интенсивных импульсов рентгеновского излучения -1 , что согласуется с ранее проведенными исследованиями HDA.
Через 8.4 нс после подачи ИК импульса образцы подверглись нагреву. В этот момент было замечено, что положение пика оставалось постоянным и близким к положению пика жидкой воды при 300 К и давлениях от 2 до 3 кбар. Через 16.8 нс на графике появляется плечо при q = 1.7 Å -1 , что аналогично положению q для LDA и LDL. Интенсивность этого пика увеличивалась по мере продолжения декомпрессии до временной задержки в 3 мс. При более длительных задержках (от 3 мс до 1 мс) наблюдалось развитие пиков Брэгга, соответствующих фазе льда Isd, которые увеличивались со временем. При окончательном измерении временной задержки (1 мс) все образцы превращались в лед.
На графике 2В показаны временные задержки для образцов толщиной от 15 до 25 мм, где степень преобразования HDL в LDL была выше, чем у образцов с большей толщиной. Спустя 1 мс соотношение двух компонентов составляет почти 1:1. Это, вероятнее всего, связано с тем, что в более тонких образцах процесс нагрева протекает более равномерно. В более толстых образцах ИК излучение поглощается больше на передней поверхности, чем на задней, что приводит к большему градиенту температур. Две наблюдаемые взаимопревращающие фазы имеют q-положения вблизи HDL и LDL, как и было предсказано на основе экстраполяции данных по зависящему от температуры и давления рассеянию нейтронов водой при более высоких температурах.
Сценарии, показанные на 1D—1F, могут быть только в том случае, если образец после ИК импульса был жидкостью, а не аморфным твердым телом, и оставался жидким во время процесса декомпрессии.
Сразу после ИК импульса образец перемещался в точку на фазовой диаграмме, лежащую выше температуры гомогенного образования льда (TH), что соответствует быстрой жидкоподобной диффузии. В этой области вода была метастабильной жидкостью в течение нескольких минут, прежде чем превратилась в кристаллические фазы льда.
Чтобы понять, как сразу после нагрева HDA ИК импульсом возникает жидкоподобная диффузия, ученые метод классической молекулярной динамики для модели воды ST2 (исследование по данной теме доступно по ссылке: Improved simulation of liquid water by molecular dynamics).
Наблюдаемое температурное смещение в 25 К означает, что экспериментальная температура 205 К соответствует
230 К для ST2 воды.
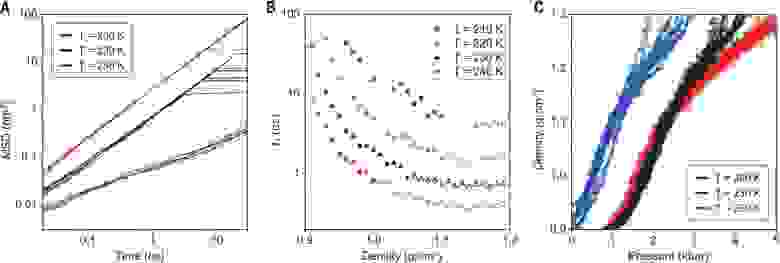
Изображение №3
На 3А показано среднеквадратичное смещение (MSD) молекул ST2 как функция времени после быстрого нагревания (при 3000 К/нс) образца HDA. Начиная с 80 К, HDA нагревали до одной из трех различных конечных температур в диапазоне от 200 до 250 К. Если бы была задержка для перехода образца в жидкое состояние, то среднеквадратичное смещение было бы изначально постоянным, а затем линейно увеличивался бы после задержки.
В ходе моделирования системы было обнаружено, что среднеквадратичное смещение увеличивается со временем линейно, как и ожидалось для диффундирующей жидкости. Из этих результатов следует, что в течение 20 пс после быстрого нагрева HDA в системе образуется жидкое состояние. Этот процесс был намного быстрее, чем частичное таяние льда фазы Ih посредством ИК импульса, которое длилось
Тем не менее травление кристаллов, т.е. переход между фазами со значимыми отличиями в структурах до и после, является процессом, требующим активации (т.е. преодоления барьера свободной энергии).
Используемые в опытах образцы льда выдерживали от 0.5 до 5 часов при температуре 115 К, потому они еще до нагрева находились в ультравязком жидком состоянии. Образцы не столкнулись с барьером свободной энергии при нагревании от 115 до 205 К. Это согласуется с тем, что HDA и HDL структурно тесно связаны, и в результате начало быстрой диффузии было моментальным.
Коэффициент диффузии (D) для жидкой воды при 205 К и 3 кбар, полученный при анализе экспериментальных данных, составил D = 2 х 10 -11 м 2 /с. Дабы преобразовать D в показатель времени для жидкоподобной диффузии, необходимо было сначала определить t1 = (1 nm 2 )/6D, где t1 — среднее время, необходимое среднеквадратичному смещению для достижения 1 нм 2 , что эквивалентно диффузии, превышающей диаметр молекулы воды в три раза. Расчеты и наблюдения показали, что сразу после ИК импульса t1 составляет 8 нс. Для ST2 модели, когда температура системы была в диапазоне от 220 до 240 К, а плотность 1.2 г/см 3 , время t1 составляло от 0.5 до 2 нс (3B). Даже после самой короткой временной задержки, образец, полученный после ИК импульса, имел достаточно времени, чтобы перейти в жидкое состояние HDL.
Временной показатель жидкоподобной релаксации в областях низкой плотности, образовавшихся в образцах при декомпрессии, можно было оценить несколькими способами. Предыдущие измерения в тонких слоях LDL воды при 1 бар и 205 К показали D = 2 х 10 -13 м 2 /с, что соответствует t1 = 800 нс. Это примерно в 100 раз больше, чем у HDL, образовавшихся после ИК импульса. В соответствии с этими данными было установлено, что для ST2 воды t1 увеличивался примерно в 50 раз, когда система преобразовывалась из чистого HDL в чистый LDL (3B). Также было выявлено моментальное изменение плотности ST2 модели при T > 200 К во время быстрой декомпрессии (3С).
Эксперименты и моделирование показали, что жидкостное равновесие системы при 205 К в LDL образовывалось за время в 50-100 раз большее, чем для HDL. Следовательно, если есть возможность достичь жидкостного равновесия в течение нескольких наносекунд, то этого же можно достичь и в течении сотен наносекунд. Если это так, то отдельные фазы с высокой и низкой плотностью, наблюдаемые в субмикросекундном временном масштабе, можно воспринимать как квазиравновесные жидкие фазы.
При учете сценариев, показанных на 1С—1Е, должно происходить быстрое преобразование в лед или непрерывное преобразование жидкого состояния. Однако этого не происходило. Образование кристаллического льда могло бы происходить в масштабах времени, более чем на один порядок превышающих преобразование в LDL. Из этого следует, что экспериментальные данные могут быть количественно согласованы только со сценарием, показанным на 1F.

Изображение №4
Дабы лучше понять, как происходит образование LLT, были проанализированы отличия в рассеянии для образцов разной толщины (от 35 до 55 мм). Это позволило оценить фракционную заселенность каждой фазы в образце как функцию временной задержки (4A).
На 16.8 нс наблюдается лишь небольшая доля LDL, которая достигала максимума (
40% от общей интенсивности рассеяния) спустя 3 мс. Этот процесс сопровождается соответствующим уменьшением доли HDL. На временной отметке в 3 мс появляется кристаллический лед, который в последствии преобладает по всей системе. Образование льда происходило во временном масштабе, более чем на один порядок превышающем переход от HDL к LDL. Это указывает на то, что LLT, хоть и является метастабильным фазовый переход, он все же отличается от перехода жидкость-лед.
Из-за динамического характера процесса декомпрессии ожидалось, что преобразование HDL в LDL будет происходить в области на графике между линией HDL-LDL сопряжения и пределом метастабильности фазы HDL. В этой области переход должен проявляться в короткие промежутки времени в виде локализованных LDL флуктуаций, за которыми следует зарождение и рост LDL доменов. На 4В (график малоуглового рентгеновского рассеяния, SAXS) отчетливо видны небольшие флуктуации LDL.
Полное преобразование образца в LDL было прервано процессом образования льда. Однако для тонких образцов соотношение HDL:LDL достигало значения 1:1 за 1 мс до появления льда (2В).
Для более детального ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых и дополнительные материалы к нему.
Эпилог
В данном труде ученые установили наличие второго жидкого состояния для воды, возникающего при 205 К. Результаты экспериментов показали, что переход жидкость-жидкость (LLT) происходит в условиях (давление и температура), при которых обычно происходит только кристаллизация.
Кроме того, наблюдаемый для LLT временной масштаб (от наносекунд до микросекунд), согласуется с предыдущей экспериментальной оценкой, основанной на экстраполяциях от 10 мс при 174 К до наносекунд и микросекунд при 220 К с использованием температурно-зависимых кинетических измерений.
Ученые отмечают, что ранее подобных наблюдений не было ввиду отсутствия соответствующего оборудования. В современных лабораториях есть возможность проводить рентгеновские исследования процессов, которые протекают молниеносно. В добавок к этому существует множество методик моделирования, позволяющих предугадать ход исследуемых процессов до фактических наблюдений. Фактор скорости крайне важен, когда речь идет об исследовании воды в момент ее преобразования в лед. За счет «быстрых» рентгеновских лучей ученым удалось наблюдать процесс преобразования одной жидкости в другую, что предшествует образованию льда. Следовательно, при определенных условиях вода из жидкого состояния переходит в другое жидкое состояние.
Результаты этого колоссального труда открывают новые возможности перед исследователями воды, позволяя разрешить многолетние споры вокруг живительной жидкости и ее необычных свойств.
В будущем ученые намерены провести дополнительные исследования своего открытия, поскольку остается еще немало вопросов касательно свойств второго жидкого состояния воды и его важности в процессах, протекающих на планете. По некоторым предположениям наличие двух жидких фаз воды может каким-то образом быть связано с биологическими процессами в живых клетках.
Благодарю за внимание, оставайтесь любопытствующими и хорошей всем рабочей недели, ребята. 🙂
Немного рекламы
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Maincubes Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 — 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB — от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
Источник







